Podezření na výskyt Cushingova syndromu neboli hyperadrenokorticismu (HAC) lze u pacientů vyslovit na základě anamnézy a klinického vyšetření. Endokrinní testy pak slouží k potvrzení tohoto onemocnění. Během posledních let se zvyšuje povědomí o výskytu této poruchy, a proto pacienti přichází spíše s mírnými symptomy. Nicméně žádné z vyšetření, ať už se jedná o biochemické testy nebo hormonální stanovení, není dokonalé. Nově mohou být určitou pomocí také zobrazovací metody, které se stávají běžnou součástí veterinárních pracovišť. V článku se členové komise odborníků zamýšlejí nad nutností přezkoumat některé referenční hodnoty používaných endokrinních testů. Jako důvod uvádějí určité změny v projevech hyperadrenokorticismu a také změny technologií používaných k vyšetření.
Zajímavá je také poslední část článku, která je věnována Syndromu atypického či Okultního hyperadrenokorticismu. Tento typ HAC lze definovat jako „stav, kdy pes vykazuje příznaky Cushingova syndromu na základě anamnézy, klinického vyšetření a klinickopatologických nálezů, ale výsledky endokrinních testů (LDDST, UCCR a ACTH stimulačního testu) spadají do normálních referenčních hodnot, jež jsou v současnosti uznávány.
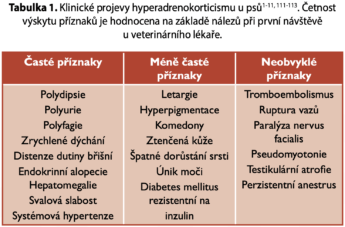
Nové informace k diagnostice Cushingova syndromuE.N. Behrend, H.S. Kooistra, R. Nelson, C.E. Reusch a J.C. Scott-Moncrieff, Překlad: MVDr. Radek KašparCelý článek v originální verzi včetně Referencí & Odkazů je k dispozici ve společnosti Cymedica. Podezření na výskyt onemocnění lze u pacientů vyslovit na základě anamnézy a klinického vyšetření. Endokrinní testy na potvrzení onemocnění je vhodné provádět pouze u psů, jejichž klinické příznaky odpovídají hyperadrenokorticismu. Žádné z vyšetření, ať už se jedná o biochemické testy nebo hormonální stanovení, není dokonalé. Určitou úlohu v diagnostice hrají i zobrazovací metody. Během posledních let se zvyšuje povědomí o výskytu této poruchy, a proto pacienti přichází spíše s mírnými symptomy. Členové komise odborníků se domnívají, že bude nutné přezkoumat referenční hodnoty používaných testů, neboť dochází ke změnám v projevech hyperadrenokorticismu a mění se i technologie používaných vyšetření. Nejasnou zůstává úloha prekurzorů kortizolu a pohlavních hormonů při vzniku syndromu okultního hyperadrenokorticismu. Klinický obraz onemocnění: indikace k provádění diagnostických testůPodezření na hyperadrenokorticismus (HAC) lze u pacientů vyslovit na základě anamnézy a klinického vyšetření. Endokrinní testy, které slouží k potvrzení onemocnění, je vhodné provádět pouze u psů, kteří vykazují klinické příznaky odpovídající HAC. Členové komise odborníků se domnívají, že vzhledem ke větším povědomí o výskytu onemocnění, se pacienti nyní objevují na klinikách v mnohem časnějších stádiích poruchy. Proto i klinické projevy HAC bývají dnes méně výrazné a prevalence klinických příznaků, jakož i nálezy během klinického vyšetření, nejsou tak markantní jako u případů publikovaných před desítkami let. Primární indikací k provedení diagnostických testů u pacientů je výskyt jednoho nebo více častých klinických projevů HAC nebo průkaz obvyklých příznaků při klinickém vyšetření (tabulka 1)1-10. Jestliže se u pacienta objevuje pouze 1 symptom HAC, bývá to obvykle polyurie a polydipsie nebo alopecie spojená s kožními změnami, jež odpovídají hormonální poruše.11 Případy HAC, které se ocitnou u dermatologa, mohou vykazovat jiný soubor příznaků než pacienti vyšetřovaní specialisty na interní medicínu. Zkratky:ACTH – adrenokortikotropní hormon ALP alkalická fosfatáza
I když se nám nepodaří objevit celý soubor příznaků onemocnění, nelze HAC vyloučit. Avšak se stoupajícím počtem projevených symptomů má i větší smysl provádět diagnostické testy. Výskyt méně častých klinických příznaků či nálezů během vyšetření slouží jako další důvod, proč bychom měli pacienta otestovat. Mezi méně časté klinické projevy HAC patří anestrus a testikulární atrofie, ochablost vazů, jež může vést k jejich natržení a kulhání12, faciální paralýza a pseudomytonie13,14. Závažná polyurie, infekce močového traktu nebo kombinace obou těchto poruch dokáže vyvolat únik moči, zvláště během spánku psů, takže majitel příznak považuje za močovou inkontinenci. Následkem zvýšené srážlivosti krve (hyperkoagulabilita) někdy vzniká spontánní tromboembolismus, který většinou postihuje pulmonární cévy a vyvolává akutní respirační útlum15,16. Rezistence na inzulin způsobená kortizolem podporuje vznik diabetu a potlačuje exogenní odpověď inzulinu17,18. Pokud u pacienta první zjistíme méně časté klinické příznaky, vyplatí se provést pečlivé zhodnocení anamnézy, výsledků klinického vyšetření i laboratorních testů, neboť pak často objevíme další důkazy pro HAC. Zásadním negativním prediktorem onemocnění je chybění symptomů popsaných v tabulkách 1 a 2. Klinické projevy se také mohou objevit sekundárně následkem vzniku tumorózní masy v hypofýze či v nadledvinách (AT – adrenální tumor). Velký nádor hypofýzy může vyvolat neurologické příznaky (syndrom pituitárního makrotumoru) zahrnující inapetenci, anorexii, stupor, manéžový pohyb, bezcílné toulání, kompulzivní pohyby končetin, ataxii a změny chování. I když se syndrom pituitárního makrotumoru objevuje u 10-25 % psů měsíce až roky po stanovení diagnózy HAC, u některých jedinců se jeho mírné příznaky mohou vyskytnout již při prvním vyšetření. Pokud prokážeme v rámci diagnostiky nervových poruch velký tumor hypofýzy pomocí počítačové tomografie (CT) či magnetické rezonance (MRI), měli bychom poté provést testování na HAC. Adrenokortikální karcinomy mohou invadovat do frenikoabdo – minální vény, kaudální duté žíly či obou. Pak vzniká retroperitoneální krvácení, anémie ze ztráty krve a bolesti dutiny břišní nebo dochází ke tvorbě nádorového trombu, jež způsobuje ascites či parézu pánevních končetin19,20. Testování na HAC se doporučuje i v případě neočekávaného nálezu masy v nadledvinách při použití zobrazovacích metod v rámci diagnostiky jiných zdravotních problémů, například zvracení. Když poté provedeme pečlivou revizi anamnézy, nálezů při klinickém vyšetření a opakované zhodnocení výsledků hematologického a biochemického vyšetření, mnohdy objevíme další projevy hyperadrenokorticismu, pokud se jedná o relevantní případ. Přítomnost AT podmiňuje způsob terapie pacienta, a proto bychom měli provést testování na HAC ještě před případnou adrenalektomií. Výsledky kompletního vyšetření krve (CBC), biochemického vyšetření, analýzy moči a stanovení poměru protein: kreatinin v moči, stejně jako měření krevního tlaku mohou přinést další podpůrné důkazy diagnózy HAC (tabulka 2). Žádná z abnormalit, které jsou seřazeny v tabulce 2, ovšem není patognomická pro HAC. Výsledky laboratorních testů a měření krevního tlaku je nutno interpretovat ve světle nálezů z anamnézy a klinického vyšetření. Pokud se u pacienta neobjevují časté abnormality popsané v tabulce 1, pravděpodobnost HAC významně klesá. Na druhé straně na základě chybění projevů, jež jsou uvedeny v tabulce 2, onemocnění rozhodně vyloučit nemůžeme. Jestliže provedeme měření žlučových kyselin, může být jejich koncentrace mírně zvýšená. Vztah příčiny a následku mezi HAC a vznikem mukocele ve žlučovém měchýři zatím nebyl prokázán. Podezření u pacientů, kde se vyskytují běžné abnormality uvedené v tabulce 1, dále stoupá v případě, že potvrdíme při vyšetření dutiny břišní ultrazvukem bilaterální adrenomegalii nebo adrenální tumor. Avšak průkaz nadledvin v normální velikosti při vyšetření ultrazvukem nelze považovat za možnost, jak vyloučit HAC. Pokud je to možné, vyplatí se neprovádět testování na HAC u závažně nemocných pacientů. Existuje mnoho onemocnění, jež ovlivňují výsledky skríningových testů na HAC21,22. Není nutné provádět testy na HAC ve chvíli, kdy se objeví podezření na tuto poruchu. Doporučuje se vyčkat s provedením endokrinních testů až do okamžiku vyléčení či kontroly současně probíhajícího onemocnění, jeho přítomnost musíme vždy i tak vzít v úvahu. Celkově lze říci, že důvody pro provedení diagnostických testů na HAC jsou následující:
Skríningové testyŽádný test nedosahuje přesnosti 100 %. Pozitivní a negativní prediktivní hodnoty testů závisí na prevalenci onemocnění. Pokud je populace pacientů, kde provádíme diagnostické testy, vybrána správně, a onemocnění má u nich vysokou prevalenci, jsou výsledky testů přesnější. Diagnostika HAC je založena na průkazu jedné z následujících dvou variant: (1) zvýšená produkce kortizolu nebo (2) snížená senzitivita osy hypotalamus-hypofýza-nadledviny (HPPA) vůči negativní zpětné vazbě na hladinu glukokortikoidů. Měření jednotlivých hodnot bazální koncentrace kortizolu nemá žádnou diagnostickou hodnotu. Pulzní sekrece adrenokortikotropního hormonu (ACTH) totiž způsobuje proměnlivost hodnot kortizolu23,24, který může i přes poruchu v některých okamžicích dosahovat fyziologických hladin. Naopak psi trpící neadrenálním onemocněním (NAI) mohou vykazovat zvýšené hodnoty bazálního kortizolu22,25. Mezi testy, jež se používají nejčastěji, patří supresní test s nízkou dávkou dexametazonu (LDDST), měření poměru kortikoidy: kreatinin v moči (UCCR) a ACTH stimulační test. Vzhledem k tomu, že všechna tato měření slouží k diagnostice HAC ve veterinární medicíně již od 70. či 80. let minulého století, navrhují členové odborné komise znovu ověřit referenční rozmezí a limitní hodnoty využívané v uvedených testech. Zaprvé platí, že naměřené hodnoty kortizolu se liší podle metodiky měření. Proto nelze hodnoty brát v potaz bez ohledu na způsob měření. Zadruhé si musíme uvědomit, že v předchozích desetiletích se změnily metody stanovení i jednotlivé testy, ale neobjevily se žádné nové referenční hodnoty. Třetím faktorem je skutečnost, že studie použité pro vytvoření referenčních hodnot nebyly provedeny správně, takže například porovnávaly skupinu pacientů s HAC se zdravými psy namísto srovnání se psy suspektně nemocnými. Mezi další problémy použitých studií patří využití malých skupin pacientů či sestavení kontrolních skupin ze psů trpících neadrenálním onemocněním, kde nebylo podezření na HAC. Navíc studie k ověření skríningových testů byly prováděny na referenčních pracovištích, kde je předpoklad vysoké prevalence onemocnění, kdežto nyní se diagnostika provádí často v běžných ordinacích u populace psů s nízkou prevalencí HAC. Začtvrté je nutno uvést, že se zřejmě v posledních letech zvyšuje výskyt zachycení mírných případů HAC vzhledem k vyššímu povědomí o této poruše a časnější návštěvě suspektních pacientů u veterinárního lékaře. U psů trpících HAC může získat negativní výsledek při jakémkoli skríningovém testu. Pokud diagnostika poskytne neuspokojivý výsledek, ale podezření na HAC přetrvává, je vhodné provést další typ testu. V případě, že se dočkáme negativního závěru u více testů, musíme zvážit skutečnost, že pacient opravdu netrpí HAC. Další variantou je situace, kdy pes může mít mírnou formu HAC a testy zatím nevycházejí pozitivně. Tehdy se vyplatí provést testy opakovaně za 3-6 měsíců, pokud dochází k dalšímu rozvoji klinických příznaků.
Stanovení kortizoluTesty na stanovení kortizolu. Celkový kortizol (vázaný nebo volný) lze měřit v séru nebo plazmě; v moči či slinách můžeme stanovit pouze volný kortizol. K dispozici jsou různé techniky měření (např. RIA, ELISA, chemiluminescence). Podle informací členů odborné komise zatím nebyly publikovány žádné údaje o měření kortizolu přímo v praxi v recenzovaném časopise, a proto tyto metody nejsou v textu uvedeny. Hladiny kortizolu v oběhu se liší podle použitého testu. Program EQUAS řízený Michiganskou státní univerzitou poskytuje srovnávací údaje o způsobu měření různých laboratoří. Například hladina kortizolu měřená metodou Immulite je vyšší než výsledky, které poskytuje RIA (Dr. R. Nachreiner, osobní komunikace). Rozdíly existují i v údajích od různých laboratoří, jež používají stejnou metodologii. Podle zprávy XXXV sestavené v rámci programu EQUAS (červenec 2010) se pohybovaly hodnoty kortizolu stanovené v 27 laboratořích ve stejném vzorku metodou Immulite v rozmezí od 3,7 do 7,2 μg/dl (101-199 nmol/l). Dalších jedenáct laboratoří používá stejnou metodu RIA; jejich hodnoty u stejného vzorku dosáhly rozmezí od 3,0 do 5,0 μg/dl (83-137 nmol/l). Typ zkumavky, druh vzorku, čas odstředění a stabilita. Koncentrace kortizolu se nezměnily, ať už byl vzorek skladován v skle nebo plastu,26 jednalo se o vzorek séra nebo plazmy,26,27 a odstředění proběhlo za 10 minut nebo 40 hodin po odběru krve27. Kortizol si udržuje stabilní hladinu v plazmě a moči při 4 či 25° C po dobu 5 dní, ale jeho hodnota se snižuje v séru při 4, 25 a 37° C (v porovnání s -20° C)26. Odborná komise doporučuje pro zajištění správné manipulace se vzorkem, aby po odstředění byl vzorek uchováván v ledničce po dobu až 24 hodin či zamražen, pokud bude měře- ní prováděno později, při teplotě -20° C. Moč lze skladovat při teplotě 4° C po dobu až 4 dní nebo při -20° C po dobu >5 dní. Vzorek je nutno odeslat do laboratoře přes noc, není podstatné, jestli se jedná o sérum nebo plazmu, a běžné balení vzorku je zcela postačující. Zkřížená reaktivita. Vzhledem ke zkřížené reaktivitě mezi různými steroidy (prednisolon, prednison, metylprednisolon, fludrokortizon, kortizon, hydrokortizon), jež je závislá i na použité metodice vyšetření, doporučují členové komise dodržet interval 24 hodin mezi poslední aplikací steroidů a měřením kortizolu. Období 24 hodin ovšem nedostačuje k vyloučení rizika adrenální suprese vyvolané sekundárně po aplikaci glukokortikoidů. Vliv hemolýzy a lipémie. Účinek lipémie a hemolýzy je rozdílný podle použitého druhu testu. Komise doporučuje kontaktovat zvolenou laboratoř a informovat se na podmínky testu, který mají. Osa hypotalamus-hypofýza-nadledviny a léky. Existuje mnoho léků, které ovlivňují aktivitu HPAA u humánních pacientů27. Mnoho těchto přípravků se ve veterinární medicíně nepoužívá, ale mezi ty užívané patří metoklopramid, klonidin, buprenorfin, kodein, klomipramin, ceruletid a desmopresin. S výjimkou desmopresinu28 nám zatím chybí studie o vlivu těchto látek na HPAA. Exogenní podávání progestinů29 a glukokortikoidů dokáže suprimovat HPAA. Délka suprese závisí na délce používání přípravku, jeho dávce, způsobu podávání, druhu syntetického steroidu (krátkodobě či dlouhodobě působící) a individuální citlivosti. Jedná se o parametr, který nelze předpovědět30. Závěry:
Supresní test k nízkou dávkou dexametazonuPrincip testu. Pomocí LDDST lze prokázat sníženou citlivost osy HPAA na negativní glukokortikoidovou vazbu, to znamená jednu ze dvou možných charakteristik diagnostiky HAC. Navíc metabolické zpracování dexametazonu může být rychlejší u psů s HAC ve srovnání se zdravými psy31. Rezistence na supresi dexametazonem ovšem není jednoznačný děj na principu „buď všechno, nebo nic“. Jedná se o kontinuální proces, takže v časných či mírných případech HAC se vyskytuje mírná rezistence, zatímco silnější rezistence bývá přítomna u pokročilejších forem HAC33. LDDST jako skríningový test. Diagnóza HAC se stanovuje na základě koncentrace kortizolu 8 hodin po podání dexametazonu. V humánní medicíně se vzhledem k možné zvýšené citlivosti na supresi dexametazonem u pacientů s mírnou formou HAC limitní hodnoty postupně snižovaly33. Jak jsme již dříve uvedli, členové odborné komise doporučují, aby hodnoty pro veterinární medicínu byly nově stanoveny každou laboratoří. Žádná limitní hodnota ovšem správně neodhalí všechny pacienty s HAC34. Uváděná senzitivita LDDST ve veterinární oblasti se pohybuje na úrovni 85 až 100 %, pro specificitu platí rozmezí 44 až 73 %6,21,22,35-43. Převrácený průběh testu, kdy koncentrace kortizolu 8 hodin po aplikaci dexametazonu byla pod limitní hodnotou, ale koncentrace 4 hodiny po podání byla zvýšená, byl popsán u 5 psů s PDH41. Protože tento průběh testu je velmi suspektní pro HAC, doporučuje se u těchto případů další testování. Forma dexametazonu, dávkování a čas podání. V první studii s LDDST bylo dosaženo nejlepšího odlišení zdravých psů od psů trpících HAC při stanovení hodnoty kortizolu 8 hodin po podání dexametazonu v dávce 0,01 mg/kg IV37. Intravenózní podání 0,01 mg/kg dexametazonu buď ve formě fosfátu sodného, nebo v podobě polyetylen glykolu poskytlo stejné koncentrace kortizolu u psů s HAC po 2, 4, 6 i 8 hodinách39. Při srovnání dexametazonu jako polyetylen glykolu, nebo fosfátu sodného nebyly zjištěny žádné rozdíly, pokud podaná dávka byla 0,01 nebo 0,1 mg/kg44. Dávku dexametazonu ve formě fosfátu sodného je nutno vypočítat na základě obsahu účinné látky. Podle Plumbova Manuálu veterinárních léčiv (7.vydání) se 1,3 mg dexametazonu v podobě fosfátu sodného rovná 1 mg dexametazonu. Vliv načasování testu a doby krmení pacienta. U psů nedochází k cirkadiánní sekreci kortizolu23. Proto předpokládají členové komise, že výsledky LDDST nejsou ovlivněny časem provedení testu během dne. Účinek krmení na hodnoty LDDST není znám. Komise nedoporučuje podávat krmení v průběhu testu. Hladovka před počátkem testu není nutná, pokud lipémie negativně neovlivňuje měření zvolenou testovací metodou. Vliv léků. Primární metabolismus dexametazonu probíhá pomocí cytochromu P450 3A4. Látky zvyšující enzymatickou aktivitu mohou urychlit klírens dexametazonu, což by mohlo vést k falešně pozitivním výsledkům. V humánní medicíně patří mezi tyto přípravky karbamazepin, fenytoin, rifampicin, barbituráty a třezalka. Ve veterinární oblasti byl prostudován pouze účinek fenobarbitalu. Dostupné důkazy nepotvrzují žádný dopad fenobarbitalu na výsledky LDDST, i když v některých případech nemusí psi léčení fenobarbitalem vykazovat supresi45-47. Závěry:
ACTH stimulační testPrincip testu a diagnostická přesnost. ACTH stimulační test hodnotí adrenokortikální rezervní kapacitu a představuje zlatý standard v diagnostice iatrogenního HAC. Vzhledem k nízké senzitivitě tohoto stanovení se test považuje za slabší variantu skríningu spontánního HAC ve srovnání s LDDST vyšetřením. Senzitivita ACTH stimulačního testu pro všechny formy spontánního HAC u psů se pohybuje mezi 57 až 95 %. Bylo zjištěno, že u psů trpících HAC v důsledku adrenálního tumoru, je senzitivita testu na úrovni 57-63 %; u psů s PDH se rozmezí uvádí 80-83 %. Specifita se pak pohybuje mezi 59 až 93 %6,21,36,43,48-51. Druh, dávkování a způsob podávání ACTH. K dispozici jsou syntetické polypeptidy obsahující prvních 24 biologicky aktivních aminokyselin ACTH, například Cortrosyn (cosyntropin) či Synacten (tetracosanctrin). Síla těchto přípravků zatím nebyla porovnána. V nedávné době se objevily na trhu injekce Cosyntropinu určené pouze k intravenóznímu podávání. U 18 zdravých psů nebyly shledány žádné rozdíly v koncentracích kortizolu po podání 250 μg Cortrosynu IM nebo Cosyntropinu IV52. V některých zemích jsou k dispozici směsné preparáty ACTH. V jedné studii nebyly prokázány žádné rozdíly v koncentracích kortizolu 60 minut po podání směsného ACTH (2,2 jednotky/kg IM) či Cortrosynu (5 μg/kg IV)53. Také nebyly zjištěny žádné rozdíly v průměrných vrcholných hodnotách kortizolu při srovnávání aplikace 250 μg Cortrosynu u zdravých psů buď IV, nebo IM54; ani při podání 5 μg/kg Cortrosynu IV nebo IM u zdravých psů či u psů s HAC55; či při IV aplikaci Cortrosynu v dávce 250 μg/na psa ve srovnání s dávkováním 5 μg/kg, obojí u psů s HAC56,57. Když byl porovnáván vliv různých dávek cosyntropinu (10, 5, 1, 0,5, 0,1, 0,05, 0,01 μg/kg) na koncentrace kortizolu u zdravých psů56-58, nejnižší dávka stimulující maximální sekreci kortizolu se pohybovala na úrovni 0,5 μg/kg IV58. Podání depotního tetraco- sactidu (250 μg/kg IM) a cosyntropinu (5 μg/kg IV) vedlo k podobné odpovědi kortizolu 60 minut po aplikaci u zdravých psů59. Avšak ani dávky cosyntropinu pod 5 μg/kg, ani podání depotního tetracosactidu nebyly ověřeny u psů s HAC. Čas odběru vzorku. K vrcholné sekrece kortizolu dochází 60-90 minut po podání Cortrosynu v dávkách 5 μg/kg či 250 μg/na psa IV nebo IM53-57. Po aplikaci 5 μg/kg IV nebyly zjištěny žádné rozdíly mezi koncentrací kortizolu za 60 a 90 minut53,55,56. Při použití 4 směsných preparátů (2,2 jednotky/kg IM) u zdravých psů byly prokázány podobné koncentrace kortizolu za 60 minut, stejně jako po podání Cortrosynu (5 μg/kg IV). Později ovšem došlo k výrazným rozdílům ve sledovaných koncentracích kortizolu53. Vliv načasování testu a doby krmení pacienta. U psů nedochází k cirkadiánní sekreci kortizolu23. Podobně jako u testu LDDST členové odborné komise nepředpokládají, že by doba provedení testu ovlivňovala jeho výsledky. Hladovka před počátkem testu není nutná, pokud lipémie negativně neovlivňuje měření zvolenou testovací metodou. Uchovávání Cosyntropinu. Cosyntropin lze připravit a zamrazit v adekvátním množství v plastových stříkačkách při teplotě -20 °C a takto skladovat po dobu 6 měsíců60. Není známo, jestli je možno zamrazit i přípravek Synacten. Podle výrobce se musí tento preparát skladovat při teplotě 2-8° C. Vliv léků. V humánní medicíně dochází ke snížení odpovědi kortizolu na ACTH při současném podávání agonistů serotoninových receptorů, progestagenů, ketokonazolu a flukonazolu, zvýšenou reakci naopak může způsobit propranolol27. Ve veterinární medicíně je známo, že supresi sekrece kortizolu mohou navodit glukokortikoidy v jakékoli formě230, progestageny29 a ketokonazol61. Žádný účinek na ACTH stimulační test nebyl potvrzen celkově ani v individuálních případech u zdravých psů léčených fenobarbitalem po dobu 862 (n=12) či 29 týdnů46 (n=12) anebo u epileptických psů léčených po dobu 1 roku45 (n=5) či >2 roky62 (n=5). ZÁVĚRY:
Kombinovaný supresní test s dexametazonem / ACTH stimulační testKombinovaný test spojuje ACTH stimulační test pro skríning a supresní test s vysokou dávkou dexametazonu pro odlišení původu onemocnění. Vzhledem k tomu, že diagnostika HAC je postavena na výsledcích ACTH stimulačního testu, vykazuje kombinovaný test nižší senzitivitu než samotný LDDST.
Poměr kortikoidy: kreatininu v moči (UCCR)Princip testu a diagnostická přesnost. UCCR poskytuje ucelený obraz o produkci kortikoidů, který koriguje změny koncentrace v krvi. Zjištění bazální hodnoty UCCR lze provádět v tandemu se supresním testem s vysokou dávkou dexametazonu (viz níže). Kombinace těchto zjištění může být výhodná, neboť potenciálně jsme schopni prokázat jak zvýšenou produkci kortizolu, tak i sníženou citlivost na zpětnou vazbu ze strany hladiny glukokortikoidů. Pokud odebereme na veterinární klinice jednotlivý, náhodný vzorek moči, pak uváděná senzitivita UCCR se v rámci diagnostiky HAC pohy- buje od 75 – 100 %21, 63-66 a specificita dosahuje 20-25 %21, 63, 64. Avšak pokud použijeme níže uvedený protokol, pak u psů, kde klinic- ké a biochemické změny odpovídají HAC, dosahuje senzitivita UCCR při vyšetření 2 základních vzorků 99% (95% konfidenční interval, 94 – 100%) a specificita 77% (95% CI, 64 – 87 %)42. U některých psů se vyskytují významné variace v hodnotě UCCR ze dne na den. V mírných případech onemocnění může být UCCR při horní hranici referenčního rozmezí 1 den a zvýšené druhý den. Protokol. Moč na vyšetření UCCR je nutno odebrat doma nejméně 2 dny po návštěvě veterinární kliniky, abychom se vyhnuli vlivu stresu67. Ačkoli lze vzorek na UCCR získat kdykoli během dne68, je vhodnější využít ranní moč, neboť ta je reprezentativním obrazem několika hodinové tvorby moči. Vliv léků a současně probíhajících onemocnění. Glukokortikoidy a jiné léky vyvolávající supresi sekrece kortizolu, jako jsou například progestageny, mohou snížit hodnotu UCCR tím, že potlačují endogenní sekreci kortizolu. Léčba fenobarbitalem neovlivňuje UCCR47. Neadrenální onemocnění může vyvolat endogenní stres a zvýšenou sekreci kortizolu. Proto musíme hodnotit vysokou hladinu UCCR u psů, kde neexistuje silné klinické podezření na HAC, velmi opatrně. ZÁVĚRY:
Rozlišovací testyJe velmi důležité odlišit PDH od AT, protože jejich léčba i prognóza jsou rozdílné. Případy spontánního HAC vyvolaného ektopickou sekrecí ACTH69 či sekrecí kortizolu způsobenou krmivem69 jsou vzácné. Biochemické testy (psí ACTH, LDDST, HDDST, suprese dexametazonem u UCCR) dokáží odlišit mezi PDH a AT, žádný test ale není přesný na 100 %. Rozlišovací testy nemá smysl provádět, pokud již nemáme pozitivní výsledek skríningového testu.
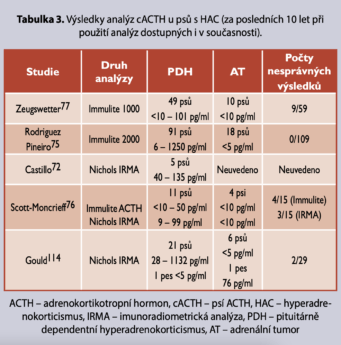
Endogenní koncentrace ACTHPrincip testu. Psí ACTH se vylučuje z hypofýzy u zdravých psů a psů s PDH epizodicky, ve vlnách23,71. Cirkadiánní rytmus sekrece ACTH nebyl přesvědčivě prokázán, i když jedna studie uvádí vyšší koncentrace cACTH v plazmě v pozdním odpoledni ve srovnání s ranní hladinou72. Hodnoty cACTH se neliší u zdravých psů a psů s PDH, proto se jejich měření nehodí ke skríningu HAC73. Měření cACTH představuje nejpřesnější samostatný biochemický test pro odlišení PDH od AT. Druhy testů na měření cACTH. Pro měření cACTH je ověřena imunoradiometrická analýza (IRMA) a chemiluminescentní metody74-77. Koncentrace cACTH zjištěné chemiluminescentní technologií jsou nižší než hodnoty získané RIA testy76. Přesnost odlišení případů PDH od AT závisí na citlivosti testu a jeho pracovním rozmezí (tabulka 3). Nejčastějším problémem při měření cACTH je špatná senzitivita. Někteří psi s PDH vykazují koncentrace cACTH na hranici či pod limitem měřitelnosti použitého testu, zvláště v případě analyzátoru Immulite 1000. Největší studie stanovení cACTH u psů s HAC využívala 2-site chemiluminescentní imunometrický test na pevné fázi (souprava Immulite ACTH a analyzátor Immulite 2000), který poskytl excelentní odlišení případů s PDH od AT75. Žádný ze psů trpících PDH nevykazoval neměřitelné koncentrace cACTH, pravděpodobně vzhledem k analytické senzitivitě testu (5 pg/ml). Rozsah cACTH hodnot u psů s PDH byl ovšem 6-1205 pg/ml a mnoho psů spadalo k dolní hranici tohoto rozmezí. Proto méně citlivé analýzy (např. Immulite 1000) zřejmě hůře odlišují jednotlivé skupiny pacientů. Variabilita v rámci jednotlivých testů i při jejich srovnání (zvýšená v případě nižších koncentrací cACTH), pulzní sekrece ACTH a nesprávná manipulace se vzorky, jež umožňuje rozklad ACTH, zvyšují pravděpodobnost falešně nízkých hodnot u psů s PDH.
Čas odběru vzorku. K dispozici nejsou žádné údaje, které by potvrzovaly, že výsledky testů či jeho rozlišovací schopnost jsou ovlivněny časem odběru vzorku. Manipulace se vzorkem. Pokud není vzorek správně ochlazen, dochází k rychle degradaci ACTH proteázami v plazmě. Krev proto odebíráme do vychlazených, skleněných zkumavek s vrchní vrstvou silikonu nebo do plastových zkumavek s EDTA, odstředíme během 15 minut (za ideálních podmínek v ochlazené odstředivce) a plazmu přemístíme do plastových lahviček k okamžitému zamrazení74,76,78. Vzorky musí zůstat zamraženy až do analýzy. Pokud používáme rychlou dopravu do laboratoře kurýrem, nezapomeňme na dostatečné množství ledu. Jestliže vzorky zasíláme, pak je to vhodné učinit přes noc zabalené se suchým ledem. Přídavek inhibitoru proteáz aprotininu (Trasylol) dokáže zabránit rozložení ACTH proteázami v plazmě74. Při použití analýzy Immulite vyvolává aprotinin umělé snížení hladiny ACTH76, takže se jeho použití nedoporučuje. Nesouhlasné výsledky testů. Někdy se objevuje nesoulad mezi koncentrací cACTH a výsledky dalších rozlišovacích testů. Mezi možná vysvětlení tohoto jevu patří epizodická sekrece cACTH, nedostatečná senzitivita analýzy nebo zhoršená kvalita vzorku. Koncentrace ACTH mohou být také ovlivněny stresem či přítomností více adrenálních poruch (např. AT se sekrecí kortizolu nebo PDH s feochromocytomem; AT a PDH se sekrecí kortizolu). Neodpovídající výsledky testu se mohou objevit i v důsledku ektopické sekrece ACTH nebo krmivem navozené sekrece kortizolu69,70. ZÁVĚRY
SUPRESNÍ TESTY S DEXAMETAZONEMPrincip testu. U zdravých psů dochází po aplikaci dexametazonu k rychlé a dlouhodobé supresi sekrece kortizolu. Při podání dexametazonu v jakékoli dávce psům s AT se žádné potlačení sekrece kortizolu neobjevuje. V případě psů s PDH, pokud je jim podána nízká dávka dexametazonu (0,01 mg/kg), nedochází k dostatečné supresi sekrece ACTH. U 75 % psů s PDH se ovšem koncentrace kortizolu snižuje po aplikaci 0,1 mg/kg dexametazonu, což je množství podávané v rámci supresního testu s vysokou dávkou dexametazonu. Zbývajících 25 % psů s PDH nevykazuje supresi ani při aplikaci vyšších dávek dexametazonu35. Pokud u psů s PDH nenastane suprese, jedná se o pacienty, kde je vyšší pravděpodobnost velkého tumoru hypofýzy32,79. Forma dexametazonu, dávkování a čas testování. HDDST analýzu je nutno provést stejně jako LDDST s tím rozdílem, že aplikujeme 0,1 mg/kg dexametazonu IV. Nedoporučuje se používat dexametazon ve formě alkoholického roztoku. LDDST a HDDST jako rozlišovací testy. Do největší studie určené ke zhodnocení obou supresních testů bylo zařazeno 181 psů s PDH a 35 psů s AT35. Postupy zvolené k rozdělení psů do skupin byly relativně přísné, ale někteří ze psů s AT reagující na mitotan mohli být začleněni do skupiny PDH pacientů. Mezi kritéria, vybraná k průkazu psů s PDH, patřila LDDST analýza s výsledkem, kdy 4 hodiny po aplikaci dexametazonu se pohybovala koncentrace kortizolu pod li- mitní hodnotou laboratoře nebo na úrovni <50 % bazální koncentrace kortizolu. Další variantou výběru byla koncentrace kortizolu 8 hodin po dexametazonu na úrovni <50 % bazální koncentrace, ale vyšší než limitní hodnota laboratoře. Kritéria pro potvrzenou supresi v rámci HDDST byla koncentrace kortizolu 4 či 8 hodin po dexametazonu, případně obojí, pod limitní hodnotou laboratoře či na úrovni <50 % bazální koncentrace. Přibližně 75 % psů s PHD splňovalo alespoň jedno kritérium suprese buď v LDDST, nebo v HDDST. Ze psů s potvrzeným PDH u 12 % nedošlo k supresi při LDDST, ale suprese byla prokázána v rámci HDDST. Rezistence na dexametazon (tzn. nesplnění žádného kritéria) se vyskytla u všech psů s AT a u zbývajících psů s PDH. Kritéria, jež byla navržena v této studii, jsou stále považována za zcela relevantní, i když nebyla provedena žádná následná studie k jejich potvrzení. V jiné studii, kde bylo zkoumáno 41 psů s AT, byl ve 28 případech proveden LDDST a u 30 pacientů HDDST6. Žádný případ suprese nebyl potvrzen. Na základě klinických zkušeností se členové odborné komise shodli, že suprese po dexametazonu potvrzuje diagnózu PDH a pes s rezistencí na dexametazon trpí buď AT, nebo PDH. Je ovšem nutno znovu vyhodnotit limitní hodnoty u těchto analýz. Suprese dexametazonem u UCCR. Snížená koncentrace kortizolu v krvi po aplikaci dexametazonu se projevuje snížením UCCR. Po odběru dvou ranních vzorků moči doma ve dvou po sobě následujících dnech se podávají tři dávky dexametazonu (0,1 mg/kg) PO v 6 až 8 hodinových intervalech a třetí vzorek moči je odebrán ráno následujícího dne. Snížení hodnoty třetího UCCR na <50 % průměru bazálních hodnot odpovídá diagnóze PDH80. Pokud se suprese neobjeví, neznamená to průkaz AT. U 160 psů s HAC (49 případů AT a 111 PDH) došlo k supresi UCCR na <50 % bazální hodnoty u 72 % psů s PDH81. Zbývajících 28 % psů s PDH bylo rezistentních na dexametazon. Psi trpící AT vykázali maximální supresi na úrovni 44 % bazální hodnoty. Nesouhlasné výsledky testů. Nesoulad mezi výsledky supresních testů a dalšími rozlišovacími analýzami se může objevit z těch samých důvodů jako při měření cACTH. Změny v metabolismu dexametazonu mohou také ovlivnit hodnoty supresních testů31,82. ZÁVĚRY
DIAGNOSTICKÉ ZOBRAZOVACÍ METODYDiagnostiku HAC nelze založit pouze na výsledcích zobrazovacích vyšetření (ultrazvuk, CT, MRI); potvrzení musí spočívat v provedení hormonálních testů. Nález normálních nadledvin při zobrazení navíc nevylučuje diagnózu HAC. RENTGENOVÉ VYŠETŘENÍPři vyšetření můžeme prokázat zvětšení dutiny břišní, zvýšený kontrast vzhledem k ukládání tuku, hepatomegalii, rozšíření močového měchýře a také mineralizaci bronchů a plicní intersticiální tkáně82. Může se také objevit mineralizace kůže a podkoží v místech predisponovaných ke vzniku calcinosis cutis. Pokud jsou játra na rentgenu malá, HAC je nepravděpodobné83. Tumor nadledvin lze vizualizovat buď prostřednictvím masy tkáně, nebo zjištěním kalcifikace tumoru. VYŠETŘENÍ ULTRAZVUKEMŠířka nadledvin představuje nejdůležitější parametr. Protože dlouhá osa nadledviny není mnohdy orientována v souladu s mediální či dorzální rovinou těla, může dojít při zobrazení průřezu žlázy k zešikmení projekce a špatnému výpočtu rozměrů orgánu. Také musíme vzít v úvahu plemeno psa a jeho tělesné rozměry. Pomocí ultrazvuku lze odhadnout velikost AT a též případnou invazi tumoru do vaskulárních struktur či měkkých tkání85,86. U psů trpících PDH obvykle nalézáme symetrické nadledviny normální velikosti či zvětšené87, může se objevit i mírná asymetrie88,89. Nálezy odpovídající AT jsou střední stupeň asymetrie, atrofie kontralaterální nadledviny (šířka nadledviny <4 až 5 mm), poškození normální tkáňové architektury či nějaká kombinace zmíněných změn. Rozlišit makronodulární hyperplazii od AT pomocí ultrazvuku může být komplikované. I když většina AT jsou unilaterální, někdy se objevují i bilaterální tumory86,90,91. V případě, že prokážeme AT, můžeme podle některých nálezů předpokládat, že se jedná o maligní tumor. Metastázy lze někdy prokázat pomocí rentgenových snímků hrudníku nebo ultrazvuku dutiny břišní. Průkaz metastáz provádíme odběrem vzorku biopsií pod kontrolou ultrazvuku. Šířka nadledviny >4 cm je silně suspektní pro maligní tumor. Tumor invadující do vena cava či přilehlých tkání můžeme prokázat ultrazvukem, ale CT92 a MRI představují citlivější techniky pro rozpoznání vaskulární invaze a detekci metastáz. Proto je v ideálním případě vhodné provést po abdominálním ultrazvuku vyšetření CT či MRI předtím, než se pustíme do adrenalektomie. Rozlišení benigní od maligní formy AT je často složité, i když máme k dispozici histopatologické vyšetření. Nedoporučuje se provádět andrenalektomii u žádného psa, kde by předtím nebyla potvrzena přítomnost AT (a atrofie kontralaterální nadledviny) pomocí ultrazvuku dutiny břišní, CT, MRI nebo kombinace těchto zobrazovacích metod. CT A MRI VYŠETŘENÍTechniky zobrazení hypofýzy. Zobrazení hypofýzy poskytuje neocenitelné informace, které se týkají různých možností terapie a prognózy. Mezi léze hypofýzy řadíme celou škálu změn od malých nahloučení hyperplastických buněk až po velké tumory5. Ani v případě, že pacient nevykazuje neurologické poruchy, nemůžeme vyloučit přítomnost pituitárního makrotumoru (tzn. nádor má průměr >1 cm, zasahuje za hranice tureckého sedla (sella turcica) nebo hodnota poměru hypofýza/mozek dosahuje >0,31)32,92. Pituitární léze mohou být relativně malé, takže i kontrastní CT a MRI dokáže identifikovat pouze hypofýzu normální velikosti u psa s PDH32,88,94-96. Posteriorní část hypofýzy je zásobena krví přímo (arteriální zásobení), kdežto přední část žlázy je krvena převážně nepřímo pomocí pituitárního portálního systému; dynamické kontrastní CT vyšetření pak využívá tento rozdíl. U psa s normální hypofýzou se první po aplikaci kontrastního média zobrazuje zadní část hypofýzy. Tato fáze zobrazení se nazývá „nástřik hypofýzy“, a pokud k ní nedochází, jedná se o atrofii posteriorní části žlázy vyvolanou kompresí pituitárním tumorem. Přemístění efektu nástřiku či jeho změněné zobrazení lze využít pro detekci a lokalizaci anteriorních pituitárních mikrotumorů97. Přítomnost mikrotumoru také indikuje dorzální přemístění či snížená intenzita signálu posteriorního laloku na T1váženém MRI98. Komise odborníků nemůže doporučit jedinou specifickou zobrazovací techniku hypofýzy, neboť výběr musíme udělat na základě dostupných možností a hledaných informací. Během času se některé pituitární tumory mění na makrotumory. Mezi varianty léčby tumoru patří radiační terapie či hypofyzektomie. Obě možnosti jsou účinnější u menších tumorů a u pacientů, kteří netrpí neurologickými poruchami, proto odborná komise doporučuje techniky na zobrazení hypofýzy využít pro všechny psy ve chvíli, kdy je diagnostikováno PDH. Jestliže klinické příznaky ukazují na pituitární makrotumor, diagnózu lze potvrdit pouze zobrazením žlázy. Zobrazovací techniky jsou nezbytné i při plánování terapie před hypofyzektomií či ozařováním. V některých případech dochází k současnému vzniku AT se sekrecí kortizolu i pituitárního tumoru99. Proto 2 členové odborné komise radí provést zobrazení hypofýzy i u psů trpících AT. Všichni členové komise pak doporučují zobrazení hypofýzy při nesouhlasných výsledcích předchozích testů (např. prokážeme AT, ale koncentrace cACTH není nízká, kontralaterální nadledvina není atrofovaná s rozměry >4 až 5 mm, nebo se část postižené nadledviny jeví normální). ZÁVĚRY
PROBLEMATIKA TZV. „OKULTNÍHO HAC“MĚŘENÍ PREKURZORŮ KORTIZOLU A ADRENÁLNÍCH POHLAVNÍCH HORMONŮSyndrom atypického či okultního HAC lze definovat jako „stav, kdy pes vykazuje příznaky HAC na základě anamnézy, klinického vyšetření a klinickopatologických nálezů, ale výsledky LDDST, UCCR a ACTH stimulačního testu spadají do normálních referenčních hodnot, jež jsou v současnosti uznávány.“ Členové odborné komise dávají přednost názvu „okultní“ před atypickým, i když si uvědomují, že v humánní medicíně je názvem okultní HAC popisováno onemocnění pacientů, kteří nevykazují typické klinické příznaky HAC, to znamená jedinců trpících subklinickým či skrytým hyperadrenokorticismem. Vzhledem k tomu, že termín „okultní HAC“ je jinak již znám, komise se uchýlila k jeho používání. Současné teorie, které mohou být nesprávné, tvrdí, že „okultní HAC“ vzniká následkem abnormální adrenokortikální sekrece pohlavních hormonů. Členové komise nevěří, že pohlavní hormony vyvolávají „okultní HAC“. Odkazujeme čtenáře na jiné zdroje100, kde se mohou dozvědět další důkazy svědčící pro i proti této teorii. Diagnostika standardního HAC se nikdy nezakládá pouze na bazální koncentraci kortizolu. Neexistují žádné důkazy, které by potvrzovaly, že měření bazálních koncentrací pohlavních hormonů v séru poskytuje spolehlivější vodítko v diagnostice adrenální dysfunkce. Proto se následující diskuze soustřeďuje na měření ACTH stimulačních hodnot, jež jsou měřítkem rezervní kapacity nadledvin. KLINICKÝ OBRAZPouze 14 případů popsaných ve veterinární odborné literatuře odpovídá výše uvedené definici101-104. Nevyplývá z nich žádný specifický fenotyp, jež by byl charakteristický pro „okultní HAC“. Ačkoli se v literatuře uvádí možná souvislost mezi syndromem náhlé získané retinální degenerace a hyperfosfatazémie (zvýšené hodnoty alkalické fosfatázy) u skotských teriérů v souvislosti se vznikem „okultního HAC“, zatím chybí jakékoli příčinné důkazy. Pokud bychom vzali do úvahy pouze koncentrace pohlavních hormonů po stimulaci ACTH, nebylo prokázáno zvýšení ani jednoho z těchto hormonů u více jak 62 % psů s retinální degenerací a žádný jednotlivý hormon nebyl konzistentně zvýšen. Podobně lze uvést, že u skotských teriérů s hyperfosfatazémií nebyla opakovaně prokázána zvýšená koncentrace žádného hormonu. Navíc při srovnání mělo zvýšenou hladinu pohlavních hormonů více skotských teriérů bez hyperfosfatazémie, než skupina psů vykazujících hyperfosfatazémii. Korelace proto neznamená vztah příčiny a následku. Indikace k diagnostickým testům. Testování „okultního HAC“ bychom neměli provádět, pokud neexistují žádné klinické signály pro testování na klasický HAC. Jestliže klinický obraz pacienta odpovídá HAC, pak primární indikací pro měření prekurzorů kortizolu a adrenálních pohlavních hormonů je situace, kdy jsme u psa provedli ACTH stimulační test nebo LDDST a všechny hodnoty kortizolu, včetně bazální, jsou pod limitem referenčního rozmezí. V případě, kdy můžeme u daného pacienta vyloučit exogenní podávání glukokortikoidů v jakékoli formě nebo aplikaci medikace, jež ovlivňuje syntézu kortizolu (např. ketokonazol), může se pak jednat o AT se sekrecí pohlavních hormonů. U těchto pacientů by dalším potvrzením diagnózy byl nález AT pomocí ultrazvuku, ale pokud se nepodaří AT vizualizovat, diagnózu i tak nemůžeme vyloučit. Sekrece progesteronu a 17α- -hydroxy-progesteronu (17OHP) nebo jiných pohlavních hormonů či prekurzorů kortizolu103,106 dokáže vyvolat supresi pituitární sekrece ACTH a následně atrofii normální adrenokortikální tkáně. Zatím byl zdokumentován vztah příčiny a následku mezi sekrecí pohlavních hormonů z AT a klinickými příznaky u pacientů103,104,107, zatímco potvrzení kauzálního vztahu mezí PDH a pohlavními hormony chybí. Navíc buňky AT se dokáží diferencovat a tak ztrácet schopnost syntetizovat enzymy působící v průběhu metabolických cest produkce hormonů. Konečným produktem hormonální syntézy pak může být pohlavní hormon či prekurzor kortizolu, ne samotný kortizol. Jestliže existuje pituitárně dependentní „okultní HAC“, pak zatím nedokážeme vysvětlit, jak a proč dochází ke změnám syntézy steroidů v adrenokortikální tkáni. Proto v případech mírných klinických příznaků doporučují členové odborné komise počkat a opakovaně testovat na klasické HAC, pokud dochází ke zhoršování symptomů. Jestliže jsou klinické příznaky na střední úrovni či závažné, je potřeba provést vyšetření dutiny břišní ultrazvukem. Pokud u pacienta zobrazíme normální nadledviny, musíme zvážit jiné diferenciální diagnózy. V případě bilaterální adrenomegálie se vyplatí provést zobrazení hypofýzy pomocí CT nebo MRI, abychom detekovali pituitární tumor vyvolávající časný HAC. Nakonec lze také zvážit variantu HAC způsobeného krmivem, neboť u těchto pacientů někdy zjišťujeme nízkou hladinu kortizolu po vylačnění. Testování pohlavních hormonů. V rámci diagnostiky „okultního HAC“ bylo doporučováno měření koncentrací pohlavních hormonů. Vhodnou variantou se jevilo stanovení celé skupiny hormonů, což zvyšuje senzitivitu a specificitu měření ve srovnání s hodnotou pouze jednoho hormonu. Zvýšené koncentrace jakéhokoli z pohlavních hormonů jsou častým nálezem, kdy zvýšená hodnota estradiolu byla zaznamenána u přibližně 40% všech souborných vyšetření provedených ze vzorků jedné referenční laboratoře108. Na druhé straně psi s NAI (neadrenální onemocnění) mohou mít zvýšené koncentrace pohlavních hormonů v porovnání se zdravými psy následkem adaptace adrenokortikální funkce na stresy spojené s chronickým onemocněním. Psi s chronickým NAI měli 14 %2121 či 36 %22 pravděpodobnost průkazu koncentrace kortizolu odpovídající HAC po stimulaci ACTH. Pacienti s neadrenálním onemocněním také mohou mít zvýšené hodnoty pohlavních hormonů. Jejich koncentrace podléhají častěji falešnému zvýšení v důsledku NAI než samotný kortizol. V jedné studii byla zjištěna signifikantní korelace mezi hladinami sérového kortizolu po ACTH stimulaci, 17OHP a kortikosteronem mezi psy trpícími neoplazií a pacienty se suspektním HAC, což naznačuje, že funkce nadledvin je zesílena jak při adrenálním onemocnění, tak při NAI, a v obou případech dochází k proporčnímu zvýšení produkce hormonů48. Specificita testů na 17OHP dosahuje nízkých hodnot mezi 59 – 70 %48,51,109. Specificita měření progesteronu byla v jedné samostatné studii stanovena na 55 %51. U 6 psů trpících buď feochromocytomem, nebo nefunkčním AT byly zjištěny zvýšené sérové koncentrace androstenedionu, progesteronu, 17OHP, testosteronu či estradiolu, případně kombinací těchto látek107. Alternativní teorie. Odborná komise uznává, že existují případy splňující kritéria „okultního HAC“. Tři členové komise proto budou i nadále testovat na „okultní HAC“ pomocí měření pohlavních hormonů ve specifických případech, kde byly vyloučeny všechny ostatní diferenciální diagnózy. K dispozici je několik vysvětlení, proč se objevují tito pacienti. Zaprvé, jak bylo již probráno výše, je nutno znovu stanovit referenční rozmezí a limitní hodnoty pro LDDST. Odborná komise předpokládá, že jejich hodnota by měla být nižší, takže někteří psi s „okultním HAC“ pak budou spadat mezi pacienty s typickým HAC. Pokud tato situace nastane, je možné, že někteří psi, jež jsou v současnosti zařazeni do kategorie mírných či časných případů HAC a vychází „normálně“ při analýze pomocí používaných hodnot, již do této skupiny (při nižších limitech) nebudou zařazeni. Zadruhé si musíme uvědomit, že u lidí je prokázána variabilní citlivost na kortizol110 a podobný efekt může existovat i u psů. Pak psi s vyšší citlivostí mohou vykazovat klinické příznaky HAC s koncentrací kortizolu, jež je v běžné populaci považována za „normální“. Správným označením takovéto poruchy by pak měl být „suspektní HAC“. Zatřetí nelze vyloučit, že psi splňující kritéria „okultního HAC“ mohou trpět vzácnými formami onemocnění, jako je HAC vyvolané krmivem. Další vysvětlení také mohou připadat do úvahy. ZÁVĚRY
SOUHLASNÉ STANOVISKO ODBORNÍKŮJournal of Veterinary Internal Medicine 2013 Americká organizace pro veterinární interní medicínu (ACVIM) vydává souhlasná stanoviska odborníků, která poskytují veterinárním lékařům v praxi nejnovější informace o patofyziologii, diagnostice a léčbě klinicky významných onemocnění malých zvířat. Členové řídící komise ACVIM jsou zodpovědní za výběr vhodných témat, oslovení odborníků z řad organizace, jež mají dostatečnou kredibilitu k sestavení stanoviska, a další kroky zajišťující důvěryhodnost celého procesu. Odborná stanoviska jsou sestavena na základně medicíny založené na důkazech, pokud je to možné. V případě, že některé stránky onemocnění zatím nejsou dostatečně prozkoumány či závěry studií si odporují, odborníci na to ve svém stanovisku upozorňují. Návrh stanoviska připravuje panel expertů a poté následuje oslovení všech členů ACVIM s žádostí o další komentáře, které mohou být zahrnuty do znění stanoviska. To je pak předáno redakci odborného časopisu Journal of Veterinary Internal Medicine, jež provede redakční úpravu písemného textu. Samotní autoři mají výhradní zodpovědnost za konečné znění souhlasného stanoviska. Celý článek v originální verzi včetně Referencí & Odkazů je k dispozici na vyžádání ve společnosti Cymedica. |