Polyglandulární syndrom vzniká v důsledku mnohočetného selhání endokrinních žláz. Jednou z prvních diagnóz byl tzv. Schmidtův syndrom, popsaný na základě přítomnosti Addisonovy choroby a lymfocytární tyroiditidy u humánního pacienta v roce 1926. Později byl rozšířen na stavy spočívající v primárním selhání dalších endokrinních žláz, jako jsou gonády, endokrinní pankreas a paratyroidní žlázy.
Článek od Dr. Sary Galac, která pracuje na Veterinární univerzitě v Utrechtu a také opakovaně přednášela v České republice, se primárně věnuje konkrétní případové studii labradora. Jednalo se o velmi zajímavou situaci, kdy byl pes odeslán na referenční pracoviště jako akutní pacient ve stavu hlubokého útlumu, slabosti a dehydratace. Majitel uváděl několikatýdenní špatný apetit a problémy se zátěží. Pes začal před dvěma dny zvracet a nežere.
Byly provedeny klasické laboratorní testy a na jejich základě stanovena diagnóza Addisonovy choroby. Pacient byl urgentně léčen, rychle se stabilizoval a 3. den byl s adekvátní terapií propuštěn. Po 8 týdnech ale nastaly komplikace, kdy byly provedeny další testy a zjištěna doplňující diagnóza – hypotyreóza. V článku jsou popisovány endokrinní funkční testy tak, jak je znáte, ale také úskalí, která vyplývají z kombinace dvou onemocnění. Dále autorka upozorňuje na situaci, kdy obě zmíněné nemoci sice patří mezi autoimunitní onemocnění, ale že to nemusí automaticky znamenat záchyt cirkulujících adrenokortikálních a tyroidních autoprotilátek. V závěru pak shrnuje prognózu tohoto konkrétního polyglandulární syndromu.
Více se dozvíte v článku od Dr. Sary Galac níže. (4 min čtení)
Polyglandulární syndrom – tyroidní a glukotyroidní deficience u psaSara Galac, DVM, PhD, klinika malých zvířat, fakulta Veterinární medicíny, Utrechtská univerzita, Utrecht, Holandsko; Přeložil MVDr. Radek Kašpar
Polyglandulární syndromPolyglandulární syndrom vzniká v důsledku mnohočetného selhání endokrinních žláz. Prototypem glandulárního syndromu je Schmidtův syndrom, popsaný na základě přítomnosti Addisonovy choroby a lymfocytární tyroiditidy u humánního pacienta (Schmidt a kol. 1926). Tento syndrom byl později rozšířen na stavy spočívající v primárním selhání dalších endokrinních žláz jako jsou gonády, endokrinní pankreas a paratyroidní žlázy.
Případová studieStav pacienta na počátku5letý pes, labradorský retrívr, byl odeslán na kliniku malých zvířat Utrechtské univerzity jako akutní pacient ve stavu hlubokého útlumu, slabosti a dehydratace. Majitel také uváděl špatný apetit a problémy se zátěží trvající několik týdnů. Před dvěma dny pes začal zvracet a přestal úplně přijímat potravu. Klinické vyšetření odhalilo letargického psa s bledými a suchými sliznicemi, slabě hmatným pulzem o frekvenci 60 úderů za minutu (BPM), dýchání bylo normální. Okamžitě byla zahájena infuzní terapie roztokem Ringer laktát s cílem potlačit hypovolemický šok. Také jsme odebrali vzorky krve a moči na rutinní laboratorní vyšetření (Tabulka 1). Závažná hyponatrémie, hyperkalémie a prerenální azotémie podporují diagnózu Addisonova choroba. Provedli jsme ACTH stimulační test a změřili koncentraci aldosteronu (ALD) v plazmě a plazmatickou aktivitu reninu (PRA). Poté byly parenterálně podány glukokortikoidy a mineralokortikoidy. Odezva na terapii byla excelentní. Tři dny po hospitalizaci pacient dobře přijímal krmivo a přestal zvracet. Koncentrace plazmatického sodíku, draslíku, močoviny a kreatininu se vrátily do normálu (Tabulka 1). Pes byl propuštěn z veterinární nemocnice s orální substituční terapií spočívající v aplikaci glukokortikoidů (kortizon acetát, 1 mg/kg/denně), mineralokortikoidů (fludrokortizon acetát, 0,0125 mg/kg/denně) a solí (chlorid sodný, 0,1 g/kg/denně). Jedinou přetrvávající abnormalitou byl nízký hematokrit. Jedním z charakteristických rysů hypokortizolémie je sekundární neregenerativní anémie v důsledku suprese kostní dřeně, proto jsme u pacienta neprováděli v daný okamžik žádnou další diagnostiku. Majitele jsme pozvali na kontrolu za 2. týdny.
V humánní medicíně se syndromy polyglandulární deficience dělí na tři odlišné typy (Eisenbarth a Gottlieb 2009): Typ I je představován pacienty, kteří trpí alespoň dvěma z triády onemocnění, což jsou Addisonova choroba, primární hypoparatyreóza a chronická mukokutánní kandidóza. V některých případech se u postižených pacientů ještě objevují různé imunitní poruchy. Typ II zahrnuje Addisonovu chorobu s autoimunitním onemocněním štítné žlázy a/nebo inzulin dependentním diabetem. Do tohoto typu nepatří pacienti s hyperparatyreózou nebo kandidózou. I tady se mohou objevit další imunitní poruchy. Toto onemocnění typu II se nazývá Schmidtův syndrom. Typ III zahrnuje autoimunitní tyroidní onemocnění spolu s dalším autoimunitním onemocněním, ale bez Addisonovy choroby. V této případové studii je popsán pacient s primární hypotyreózou a primární adrenokortikální deficiencí, což je podobné polyglandulárnímu autoimunitnímu syndromu typ II nebo Schmidtovu syndromu.
Mezitím nám laboratoř dodala výsledky endokrinních testů (Tabulky 2 a 3). Hodnota bazálního kortizolu byla těsně nad úrovní detekce a po aplikaci syntetického ACTH (Synacthen®, 0,25 mg) nedošlo téměř k žádné stimulaci. Tento výsledek ukazuje na vyčerpání rezervní kapacity kůry nadledvin a potvrzuje hypokortizolémii. V souladu s nedostatkem glukokortikoidů byla výrazně zvýšená bazální plazmatická koncentrace ACTH, což je fyziologická odpověď hypofýzy na nízkou úroveň negativní zpětné vazby. Bazální plazmatická koncentrace ALD byla nízká, ale stále spadala do referenčního rozmezí, takže se nepotvrdila v tomto případě mineralokortikoidní deficience.
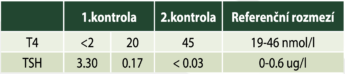
Rutinní laboratorní vyšetřní při přijetí pacienta, propuštění z nemocnice a při dvou kontrolách. Při druhé kontrole bylo také provedeno stanovení T4 a TSH.
PRA bylo závažně zvýšené, což lze vysvětlit zpětnovazební reakcí v důsledku sekundární hypovolémie vyvolané nízkou plazmatickou koncentrací ALD. Nakonec jsme spočítali poměr ALD/PRA a tak jsme mohli stanovit případný nedostatek mineralokortikoidů.
Koncentrace celkového tyroxinu v plazmě (T4) a hormonu stimulujícího štítnou žlázu (TSH) krátce před a během léčby l-tyroxinem.
Plazmatická koncentrace kortizolu (kortizol 0) před podáním Synacthenu (syntetický adrenokortikotropní hormon (ACTH)) a 60 minut poté (kortizol 60), bazální plazmatická koncentrace ACTH, aldosteronu (ALD) a plazmatická aktivita reninu (PRA).
Při první kontrole majitel uváděl, že pes je v pořádku. Má dobrý apetit, pije o něco více a mírně přibral. Pes byl pozorný, ale stále přetrvávaly problémy se zátěží. Klinické vyšetření bylo bez nálezu, pouze sliznice stále vykazovaly bledší barvu. Odebrali jsem krev na laboratorní vyšetření. Plazmatický sodík i draslík byly stále v normě, přetrvávala ovšem neregenerativní anémie. Vzhledem k tomu, že se mohlo jednat o následek nedostatku glukokortikoidů, zvýšili jsme dávku kortizon acetátu na 1,25 mg/kg/den.
Pokračování Addisonovy chorobyZa 8 týdnů přišel majitel se psem na 2.kontrolu. Opět uváděl, že pes vykazuje dobrý apetit a mírně přibral. Stále ještě přetrvávaly problémy se zátěží. Dávka kortizon acetátu musela být před několika týdny snížena na 0,75 mg/kg/den vzhledem k polyurii a polydipsii. Při snížené dávce pes pil normálně. Při klinickém vyšetření bylo zjištěno, že pes je obézní a má matnou a suchou srst spolu s alopeciemi na trupu. Kůži měl ztluštělou a na hlavě (Obrázek 1) a na končetinách vytvářela záhyby. Pacient měl slabý pulz s frekvencí 80 BPM, sliznice byly bledé a narůžovělé. Další abnormality nebyly zjištěny. Vyšetření krve prokázalo normální hodnoty ledvinných parametrů i plazmatické koncentrace sodíku a draslíku (Tabulka 1), takže jsme učinili závěr, že dávka mineralokortikoidů je odpovídající. Vzhledem k problémům se zátěží a hematokritem pod referenčním rozmezím se zdálo, že množství podávaných glukokortikoidů je stále příliš nízké. Protože ovšem vyšší dávky kortizon acetátu vyvolaly polyurii a polydipsii, nebylo pravděpodobné, že pacient trpí nedostatkem glukokortikoidů a rozhodli jsme se vzít v úvahu i jiné diferenciální diagnózy. Velmi typickými příznaky pro hypotyreózu byly změny faciálního výrazu, alopecie na trupu a slabý pulz. Toto onemocnění by také mohlo vyvolat problémy se zátěží a neregenerativní anémii. Proto bylo provedeno měření celkového tyroxinu v plazmě (T4) a hladiny hormonu stimulujícího štítnou žlázu (TSH). Přesvědčivým potvrzením diagnózy hypotyreóza byly výsledky ukazující nízkou plazmatickou koncentraci T4 a zvýšenou koncentraci TSH v plazmě (Tabulka 3). Zahájili jsme terapii l-tyroxinem (Forthyron®) v dávce 10 μg/kg hmotnosti dvakrát denně a o 6 týdnů později byl pacient opětovně vyšetřen.
Pokračování hypotyreózyMajitel uváděl, že zhruba po 2 týdnech zahájení terapie l-tyroxinem byl pes aktivnější a měl větší chuť do pohybu. Při klinickém vyšetření byla zjištěna obezita, ale kůže se hodně zlepšila. Došlo k opětovnému nárůstu srsti a kožní záhyby již nebyly tak patrné. Žádné další abnormality nebyly zjištěny. Vyšetření krve odhalilo plazmatickou koncentraci T4 zhruba 4 hodiny po podání l-tyroxinu na úrovni 35 nmol/l a koncentraci TSH v plazmě dosahující 0,23 μg/l. Hematokrit se zvýšil na hodnotu 0,40 l/l od poslední kontroly a téměř dosáhl hodnot referenčního rozmezí. Nálezy jsme zhodnotili jako pozitivní účinek l-tyroxinu u pacienta, ale protože TSH bylo stále relativně vysoké, zvýšili jsme úvodní dávku na 15 μg/kg hmotnosti dvakrát denně. Majitele jsme požádali, aby přišel na kontrolu o 4 týdny později. Při této kontrole již dosáhla plazmatická koncentrace T4 zhruba 4 hodiny po aplikaci l-tyroxinu hodnoty ve fyziologickém rozmezí (42 nmol/l) a plazmatická koncentrace TSH byla dostatečně snížena (<0,1 μg). Náš závěr byl takový, že dávka l-tyroxinu je odpovídající. Hematokrit se normalizoval, což nepřímo prokázalo, že neregenerativní anémie u tohoto pacienta byla spojena s Addisonovou chorobou a hypotyreózou.
DiskuzeTato případová studie popisuje psa s Addisonovou chorobou a hypotyreózou, což jsou dvě imunitně zprostředkovaná onemocnění. Úvodní klinický obraz pacienta výrazně napovídal, že se jedná o primární hypoadrenokorticismus neboli Addisonovu chorobu, tzn. nedostatek glukokortikoidů (letargie, problémy se zátěží) a mineralokortikoidů (hyponatrémie a hyperkalémie). Zlatým standardem diagnostiky Addisonovy choroby je ACTH stimulační test, ale tento test zjišťuje pouze adrenální zásoby glukokortikoidů. Na potvrzení deficience mineralokortikoidů je nutno změřit plazmatické hodnoty ALD a PRA. Bazální plazmatický ALD se u našeho pacienta překrýval s hodnotami, které lze změřit u zdravých psů, což je nález zdokumentovaný již dříve (Javadi a kol. 2005). Spočítáním poměru mezi ALD a PRA, což odpovídá páru hormonů podílejících se na zpětnovazebném systému, dokážeme stanovit diagnózu deficience aldosteronu, jak to krásně ilustruje náš pacient. V případě podezření na Addisonovu chorobu je zásadní provést endokrinní diagnostické testy a potvrdit či vyvrátit onemocnění (Galac a kol. 2010). Terapii Addisonovy choroby pomocí glukokortikoidů a mineralokortikoidů lze zahájit okamžitě po odebrání krve na endokrinní testy. Výsledky totiž nejsou hned. Když později zjistíme, že pacient netrpí Addisonovou chorobou, lze terapii zastavit bez jakýchkoli následků. Jestliže se stav pacienta dramaticky zhoršuje navzdory využití infuzní terapie, není už vhodné ztrácet čas endokrinními testy. Dexametazon je jediným glukokortikoidem, který neovlivňuje test na kortikoid a jeho podání stále ještě umožňuje provést seriózní testy, což můžeme učinit později, až je pacient lépe stabilizovaný. Orální medikace u našeho psa zahrnovala kortizon acetát (glukokortikoid), fludrokortizon acetát (mineralokortikoid) a sůl. Přidání soli do terapie umožňuje pružně upravit dávku mineralokortikoidů na základě elektrolytových hodnot v plazmě. Využití soli ovšem není vždy nutné (Kintzer a Peterson 1997). Úprava dávky glukokortikoidů probíhá většinou podle odebrané anamnézy při kontrole pacienta. V případě zjištění polyurie a polydipsie, případně polyfagie, což jsou klinické příznaky spojené s hyperkortizolémií, je nutno dávku kortizon acetátu snížit. Pokud se u pacienta neobjevují žádné příznaky hypokortizolémie (letargie, inapetence, problémy se zátěží), dávku je potřeba zvýšit. V předložené případové studii došlo u psa k polyurii a polydipsii, což ukazuje na hyperkortizolémii a dávku kortizon acetátu jsme museli snížit. U současně se vyskytujících problémů se zátěží jsme měli jiné podezření. Teoreticky může nadměrné působení glukokortikoidů vést k nastartování začarovaného kruhu, který začíná zvýšeným apetitem s následnou obezitou a pak nastává nechuť/neschopnost pohybu, to ale nevysvětluje zjištěnou neregenerativní anémii. Proto v tento okamžik bylo potřeba pokračovat v diagnostice. Pacient s oteklým vzhledem, tragickým faciálním výrazem, slabým pulzem, symetrickou alopecií, neregenerativní anémií a problémy se zátěží patří k typické plejádě klinických příznaků hypotyreózy, takže diagnostikovat toto onemocnění nebylo obtížné. Změřená nízká koncentrace T4 v plazmě a současně vysoká hodnota TSH stačily u tohoto pacienta k potvrzení primární hypotyreózy. Celkově lze říci, že asi u 1/3 případů primární hypotyreózy se plazmatická koncentrace TSH pohybuje ve fyziologickém rozmezí (Rijnberk a Kooistra 2010). Po určitých výzkumech směřujících k vysvětlení tohoto fenoménu prokázaly experimentální práce, že vyvolání primární hypotyreózy způsobuje úvodní zvýšení plazmatické koncentrace TSH, následně ovšem dochází k postupnému vymizení zpětněvazební odpovědi TSH na nízkou koncentraci T4. Tento jev je doprovázen hypersekrecí růstového hormonu (GH) a hyposekrecí prolaktinu (Diaz Espineira a kol. 2007). Také dochází k některým změnám hypofýzy včetně jejího zvětšení. Podobné změny lze pozorovat u psů s přirozeně se vyskytující hypotyreózou. Výsledky těchto studií poskytují vysvětlení, proč nemusí být TSH zvýšené u psů s hypotyreózou, ale neřeší diagnostické dilema. V případě klinických příznaků odpovídajících hypotyreóze a normální hodnotě TSH lze provést TSH stimulační test nebo radioizotopové vyšetření s pertechnetátem. Nevýhodou TSH stimulačního testu je v tuto chvíli fakt, že jediným dostupným TSH je rekombinantní humánní (rh)TSH, které není levné. Tyroidní scintigrafii lze provést pouze na specializovaných pracovištích (Rijnberk a Kooistra 2010). Jak přirozená produkce T4, tak parenterálně podané náhradní dávky l-tyroxinu dosahují množství zhruba 5 μg/kg hmotnosti a den k navození eutyroidního stavu. Pokud je ovšem l-tyroxin podáván orálně, je jeho biologická dostupnost nízká a variabilní vzhledem k nekompletní a měnící se absorpci v gastrointestinálním traktu. Studie u psů prokázaly, že plazmatická hladina T4 se zvyšuje po orálním podání, dosahuje maximální hodnoty o zhruba 4–6 hodin později a pak klesá až do okamžiku, kdy je podána další dávka (Kaptein a kol. 1993). Biologickou dostupnost musíme brát do úvahy při následujících kontrolách pacienta. Pokud odebereme krev 10–12 hodin po aplikaci l-tyroxinu, plazmatická koncentrace T4 by měla být nad dolní hranicí fyziologického rozmezí a v době 4 hodiny po podání poslední dávky přípravku má dosahovat k horní hranici fyziologického rozmezí. Mimo měření plazmatické T4 je potřeba stanovit i koncentraci TSH. Jestliže je suplementace l-tyroxinem dostatečná, plazmatická koncentrace TSH by měla být nízká. Addisonova choroba a primární hypotyreóza patří mezi autoimunitní onemocnění. V této případové studii nebyly měřeny žádné cirkulující adrenokortikální a tyroidní autoprotilátky. V podobné práci publikované dříve nebyly autoři schopni prokázat tyto protilátky pomocí imunofluorescence (Kooistra a kol. 1995). Proto je otázkou, jestli se vyplatí stanovit protilátky v rámci časné diagnostiky imunitně zprostředkovaných endokrinních onemocnění. Dalším problémem je zjistit, v kolika případech povede přítomnost protilátek nakonec k samotnému onemocnění. Je potřeba zdůraznit, že autoimunitní polyglandulární syndrom představuje u psa vzácnou chorobu. Proto je zřejmě jednodušší vysvětlit majitelům klinické příznaky autoimunitního onemocnění a provádět pravidelné laboratorní kontroly než začít screening celé populace na přítomnost cirkulujících autoprotilátek.
ZávěrHypotyreóza patří k onemocněním, jejichž léčba je velmi vděčná a dlouhodobá prognóza je excelentní. U Addisonovy choroby musíme léčbu upravit, pokud pacient zažívá stres. V případě, že není schopen či nemůže přijímat krmivo, je pak nutno aplikovat terapii parenterálně v injekční formě. Addisonova choroba má však také dobrou prognózu. Případy z minulosti ukazují, že například bývalý americký prezident J.F. Kennedy trpěl hypotyreózou i Addisonovou chorobou a prožil s těmito dvěma onemocněními velmi úspěšný a zajímavý život (Mendel 2009). |